直径不到120纳米的小小病毒,是如何在人体开展“攻击T细胞计划”的?
直径不到120纳米的小小病毒,是如何在人体开展“攻击T细胞计划”的?
1981年6月5日,美国疾病预防控制中心公布了5例卡氏肺孢子虫肺炎病例,他们的症状十分类似:持续高烧、体重明显减轻、免疫系统几乎完全崩溃……几个月后,一种新的传染病开始进入人们的视野,它就是获得性免疫缺陷综合征——即艾滋病(AIDS,Acquired Immunodeficiency Syndrome)。这几例特殊的病例,成为世界上第一次有关艾滋病的正式记载。
四十余年过去,艾滋病依旧是人类面临的健康挑战。据联合国艾滋病规划署最新发布报告显示,全球目前有约3900万人感染艾滋病病毒(HIV,Human Immunodeficiency Virus),仅2022年,全球新增约130万名艾滋病病毒感染者。艾滋病之所以让人闻风丧胆,就在于艾滋病毒侵入人体后,会直接侵入人体的免疫系统。这一小小病毒究竟是如何对人体免疫系统发起攻击的?未来我们有可能完全治愈艾滋病吗?
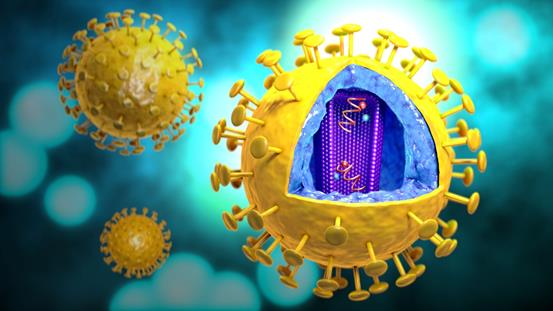
艾滋病病毒颗粒示意图
图片来源:
https://www.cdc.gov/nchhstp/newsroom/multimedia-resources/hiv-multimedia-resources.html
01 艾滋病病毒(HIV)的侵入机制
艾滋病病毒,学名为“人类免疫缺陷病毒”。直径约100~120纳米,呈圆形或卵圆形。它的基因组是两条相同的单股正链RNA。相比于DNA的双链结构,RNA的单链结构更容易发生基因变异。HIV的侵入机制涉及一系列复杂的生物学过程,它使病毒能够进入宿主细胞并开始复制:
(1)入侵宿主细胞
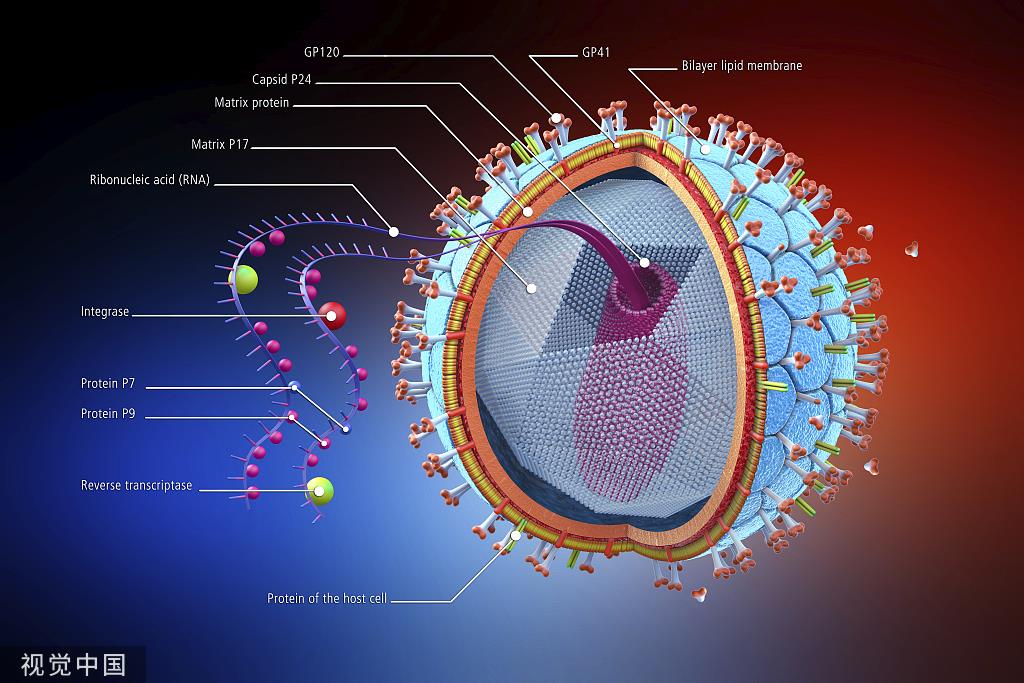
HIV攻击的主要目标是人体免疫系统中最重要的CD4+T淋巴细胞。首先,结合宿主细胞表面受体:HIV的外膜上有一种蛋白质叫做gp120,它能够与宿主细胞表面的CD4受体结合。这是病毒侵入的第一步。
与辅助受体结合:除了与CD4受体结合,HIV还需要与宿主细胞表面的辅助受体结合,以便更牢固地侵入细胞。最常见的辅助受体是CXCR4或CCR5。不同的HIV毒株可能使用不同的辅助受体。
图库版权图片,不授权转载
(2)发起疯狂进攻
接下来,HIV继续“冲锋陷阵”,一旦与CD4受体和辅助受体结合,它会经历一个融合过程,其中病毒的外膜与宿主细胞的膜融为一体。这使得病毒如“伪装大师”一般,将其遗传物质(RNA)注入宿主细胞内部。
HIV携带着一种逆转录酶(reverse transcriptase),当病毒的遗传物质进入宿主细胞内,就迅速借助逆转录酶将其转录成DNA,如同产生了新的病毒“副本”,接下来病毒DNA在另一种酶(整合酶,integrase)作用下,将其整合到宿主细胞的基因组中。这个整合到宿主DNA中的病毒DNA被称为“前病毒”。
就这样,HIV开始在体内大肆繁殖、生根发芽。这些“前病毒”被活化而进行自身转录,形成病毒RNA,同时在蛋白酶的作用下合成病毒的结构和非结构蛋白,这些新的病毒成分最终会组装成新的HIV病毒颗粒,准备感染其他宿主细胞,特别是CD4+T淋巴细胞,导致感染的扩散和免疫系统的逐渐损害。
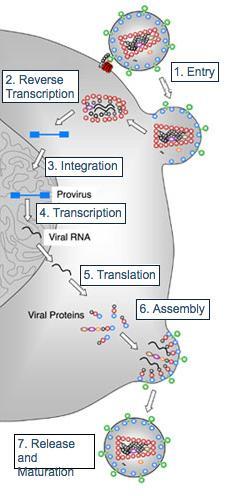
HIV病毒复制过程 来源:性病艾滋病预防控制中心
HIV进攻的过程看似如“洪水猛兽”,但对于感染者的临床症状而言也可算是一个“相对漫长”的过程。
在感染初期(急性感染期),许多人可能没有明显的症状,但此时HIV已经在体内迅速复制,少部分感染者也可能出现发热、畏寒、皮疹、乏力等类似感冒的症状。但谁偶尔没个头疼脑热呢?这些症状常常被人忽视,无疑给了HIV肆虐的机会。
在急性感染期之后进入无症状期,这个阶段可能持续数年甚至十年以上。在此期间,病毒持续复制,但症状可能不明显。这时的病人被叫作“无症状HIV感染者”。虽然看似与正常人并无异样,但此刻病毒依旧在疯狂繁殖,破坏人体免疫功能,如果未接受治疗,HIV感染最终可能会发展成艾滋病。
艾滋病是免疫系统功能受损严重的状态,由于人体细胞免疫机能已经难以维持,感染者对外界病毒、细菌完全失去抵抗能力,也就进入HIV感染的最后阶段,即“艾滋病期”,患者极容易发生严重的机会性和恶性肿瘤。
02 全球已出现数例艾滋病治愈者,攻克艾滋病的方法可复制了?
HIV的“攻占T细胞计划”是一个复杂而狡猾的过程,这个复杂的侵入机制使得艾滋病毒能够持续感染和破坏宿主的免疫系统,导致免疫系统失调和艾滋病的发展。但科研人员一直在努力研究这一过程,并寻求新的方法来预防感染和治疗艾滋病。
随着艾滋病防治领域的科技进展,以艾滋病抗病毒药物为核心的生物医学干预措施逐步发展和完善,可以有效抑制HIV的复制,减缓疾病的进展,提高患者的生活质量,并减少病毒的传播。由于抗病毒治疗的有效性提高,艾滋病的预后得到了显著改善。许多患者能够长期维持健康状态,被称为“长期抗逆转录病毒携带者”(Long-Term Non-Progressors,LTNP),他们不会迅速发展为艾滋病。
“黄金72小时自救”又称艾滋病病毒暴露后预防(Post-exposure Prophylaxis,PEP),就是一种利用抗病毒药物阻断艾滋病病毒暴露后传播的生物医学干预措施,是艾滋病综合干预策略的重要组成部分。暴露后预防为处于HIV高暴露风险的人群提供了紧急阻断的机会,有助于减少艾滋病感染和传播。目前已经在全球广泛推广应用。
而就在今年7月20日,根据美国广播公司网报道,法国和瑞士的研究人员确认了最新一名的HIV长期缓解男子,该男子被称为“日内瓦病人”,这也是全球第6位实现长期缓解的艾滋病患者。更令人感到乐观的是,他并没有接受与前五例病人同样采用的带有对HIV具有抵抗作用的CCR5△32基因突变的异体骨髓移植手术,这不禁让人猜想,是否意味着可以有更多的治疗手段来对抗艾滋病的“魔咒”?

图源:IAS 2023((International AIDS Society,国际艾滋病协会))
这名被称为“日内瓦病人”的HIV患者,实现了长期缓解,且没有接受传统的基因移植手术,这表明治疗艾滋病的途径可能更多样化和个体化。多年来,抗病毒药物的使用显著改善了艾滋病患者的生存状况,但治愈仍然具有挑战性。病毒高度变异,通用疗法不易实现。因此,科学家们探索基因治疗、免疫疗法等新策略,以期实现更多患者的长期缓解或治愈。
“日内瓦病人”的案例突显了多元化治疗的前景,不仅仅依赖传统方法。这种个性化治疗可能更好地满足不同患者需求。尽管道路漫长,但艾滋病治疗领域充满希望,科学家们将坚持努力,最终克服这一全球性挑战。新的治愈案例和研究成果为未来带来了光明,让患者有望过上健康幸福的生活。
HIV的传播不仅限于性行为,还包括母婴、血液等途径传播。此外,早期诊断对于及早开始抗病毒治疗、减少 HIV传播风险以及提高患者的生活质量至关重要。

图库版权图片,不授权转载
今天是第36个世界艾滋病日。通过普及健康教育,采取适当的预防措施如使用避孕套、避免共用注射器、接受HIV测试以及提供母婴预防措施等,我们可以减少歧视、恐慌和病毒传播,从而更好地控制和预防艾滋病。
参考文献:
[1] Centers for Disease Control (CDC). Persistent, generalized lymphadenopathy among homosexual males. Morbidity and Mortality Weekly Report.. 1982 May 21;31(19):249-51.
[2] Centers for Disease Control (CDC). Update on acquired immune deficiency syndrome (AIDS) – United States. Morbidity and Mortality Weekly Report. 1982 Sep 31 (37): 507–08, 513–14.
[3] http://www.unaids.org.cn/
作者:唐伟 长沙市第一医院感染与免疫科副主任医师
审核:李南南 湖南省科协二级调研员,湖南省科普作家协会理事,科普中国专家
陈岳飞 研究员,湖南省科普作家协会会员 ,科普中国专家
出品:科普中国
监制:中国科学技术出版社有限公司、中科数创(北京)数字传媒有限公司
标签: